- 最新进展
- 产品信息
什么是PLGF?其与子痫前期有何关联?
胎盘生长因子(PLGF)是一种由滋养细胞分泌的糖基化二聚体蛋白,属于血管内皮生长因子(VEGF)家族。它与VEGF受体1(VEGFR-1)结合,在妊娠期间表达量显著上升。PLGF通过促进胎盘血管生成和子宫螺旋动脉重铸,在维持正常妊娠中发挥关键作用。然而,在子痫前期(PE)患者中,PLGF水平显著降低,这与其发病机制密切相关。研究表明,PLGF不仅是预测子痫前期的敏感指标,还为早期干预提供了重要依据。
PLGF如何参与子痫前期的发生机制?
PLGF在妊娠不同阶段具有动态表达特征。妊娠5-15周时,PLGF呈低水平表达;15-26周急剧上升,并于26-30周达到峰值,之后逐渐下降。这一变化与胎盘供氧需求及功能成熟密切相关。在正常妊娠中,PLGF通过促进滋养细胞增殖、侵袭和子宫螺旋动脉重铸,建立有效的胎儿-胎盘循环网络。然而,子痫前期患者PLGF水平明显下降,导致螺旋动脉重铸不足、胎盘灌注减少,进而引发高血压、蛋白尿等临床症状。
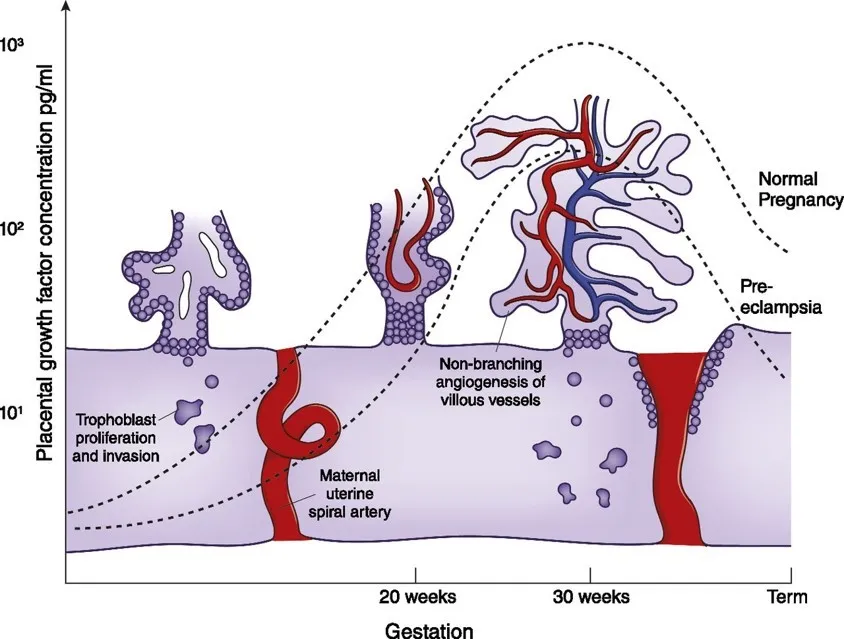
PLGF如何通过调控血管生成影响妊娠?
PLGF主要通过两种机制促进血管生成:一是通过与巨噬细胞膜受体Flt-1结合,募集并活化巨噬细胞,释放血管生成因子;二是通过作用于内皮细胞膜受体Flt-1,维持细胞生存并刺激其迁移与增殖。然而,子痫前期患者体内高水平的可溶性fms样酪氨酸激酶-1(sFlt-1)会竞争性结合PLGF,抑制其促血管生成功能,最终导致胎盘血管网络构建异常。
PLGF如何促进血管舒张与胎盘血流灌注?
在正常妊娠中,PLGF与滋养层细胞受体Flt-1结合后,通过激活一氧化氮合成酶(eNOS)促进L-精氨酸转化为一氧化氮(NO),从而诱导血管舒张,增加胎盘血流灌注。而在子痫前期患者中,sFlt-1水平升高抑制了PLGF与受体的结合,同时精氨酸酶II的过量表达降低了L-精氨酸浓度,导致eNOS生成超氧化物阴离子而非NO,进一步减少血管舒张功能,加剧胎盘缺血和缺氧。
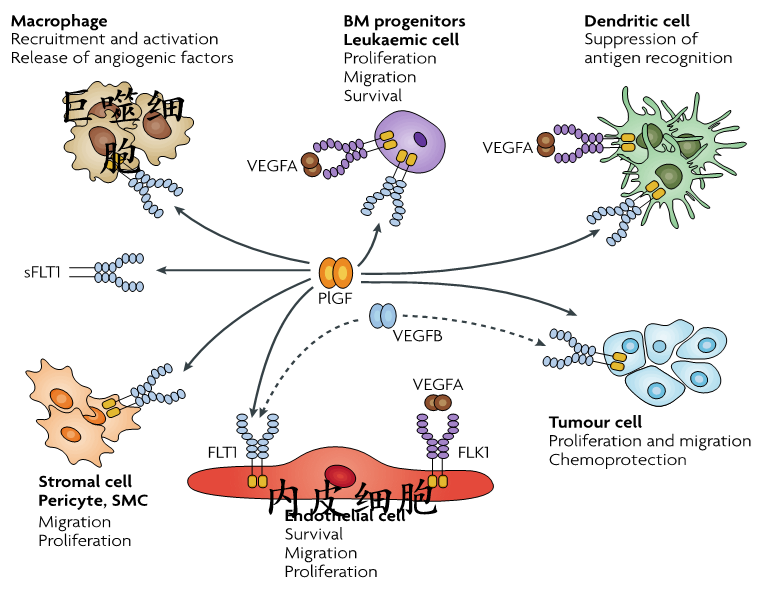
PLGF作为预测子痫前期的生物标志物有哪些循证医学支持?
自1991年PLGF cDNA首次从人类胎盘分离以来,多项研究确立了其作为子痫前期预测标志物的重要性。1998年的一项研究发现,子痫前期患者血清PLGF水平显著低于正常孕妇。2004年《新英格兰医学杂志》发表的研究表明,PLGF水平在妊娠13-16周即出现下降,比临床症状早9-11周。2010年多中心研究进一步证实,PLGF对子痫前期的预测具有高灵敏度(AUC=0.92)。2019年《柳叶刀》发表的一项大规模随机对照试验显示,PLGF检测可将子痫前期的诊断时间从平均4.1天缩短至1.9天,并显著降低严重并发症发生率。
国际指南如何评价PLGF在子痫前期筛查中的作用?
国际妇产科联盟(FIGO)在2019年指南中明确指出,PLGF是妊娠早期筛查子痫前期的最佳生化标志物。尤其对于早发型子痫前期,仅依靠母体PLGF浓度即可达到56%的检出率(假阳性率仅为9%)。此外,PLGF检测在疑似子痫前期患者的鉴别诊断和早产风险预测中也显示出重要价值。
PLGF检测在临床实践中有何重要意义?
PLGF检测不仅能够提前识别子痫前期高风险人群,还为临床干预提供了时间窗口。通过早期监测PLGF水平,医生可以及时采取预防措施,如低剂量阿司匹林治疗,从而改善母婴结局。此外,PLGF结合超声多普勒检查、血压监测等多项指标,可进一步提高子痫前期预测的准确性和可靠性。
总结:为什么PLGF被认为是子痫前期风险评估的最佳生物标志物?
PLGF因其在胎盘血管生成和螺旋动脉重铸中的关键作用,以及与子痫前期病理机制的密切关联,成为预测该疾病的最佳生物标志物。其动态变化特征和高灵敏度使其在早期筛查、风险分层和临床干预中具有不可替代的价值。随着研究的深入和检测技术的进步,PLGF有望在全球范围内助力降低孕产妇和婴儿死亡率,实现“健康中国2030”的战略目标。












