- 最新进展
- 产品信息
1. GPC3是什么?其基因与蛋白结构有何特点?
GPC3(Glypican-3)是一种位于细胞膜表面的糖蛋白,属于硫酸乙酰肝素蛋白聚糖家族。其基因定位于人类X染色体q26.1区域,编码一种由580个氨基酸组成、分子量约70 kDa的蛋白。GPC3在结构上可分为40 kDa的N端亚基和30 kDa的C端亚基,两者通过二硫键连接。该蛋白通过糖基磷脂酰肌醇(GPI)锚定在细胞膜外表面,并可在呋喃样转化酶作用下于Arg358–Ser359位点发生酶切,形成具有生物活性的异二聚体结构。这一独特结构使GPC3在细胞信号转导和微环境调控中扮演重要角色。
2. GPC3在HCC中的信号通路机制是怎样的?
在肝细胞癌(HCC)中,GPC3通过调控多条信号通路促进肿瘤发生与发展。它可与Wnt、Hedgehog、成纤维细胞生长因子(FGF)及胰岛素样生长因子(IGF)等信号分子相互作用,增强这些通路的活动。例如,GPC3通过与Wnt蛋白结合,稳定β-catenin并促进其核转位,从而激活下游增殖相关基因的转录。此外,GPC3还可抑制BMP和TGF-β等抑癌信号通路,进一步为肝癌细胞的无限增殖提供条件。这些机制使GPC3成为HCC发生中的关键分子推手。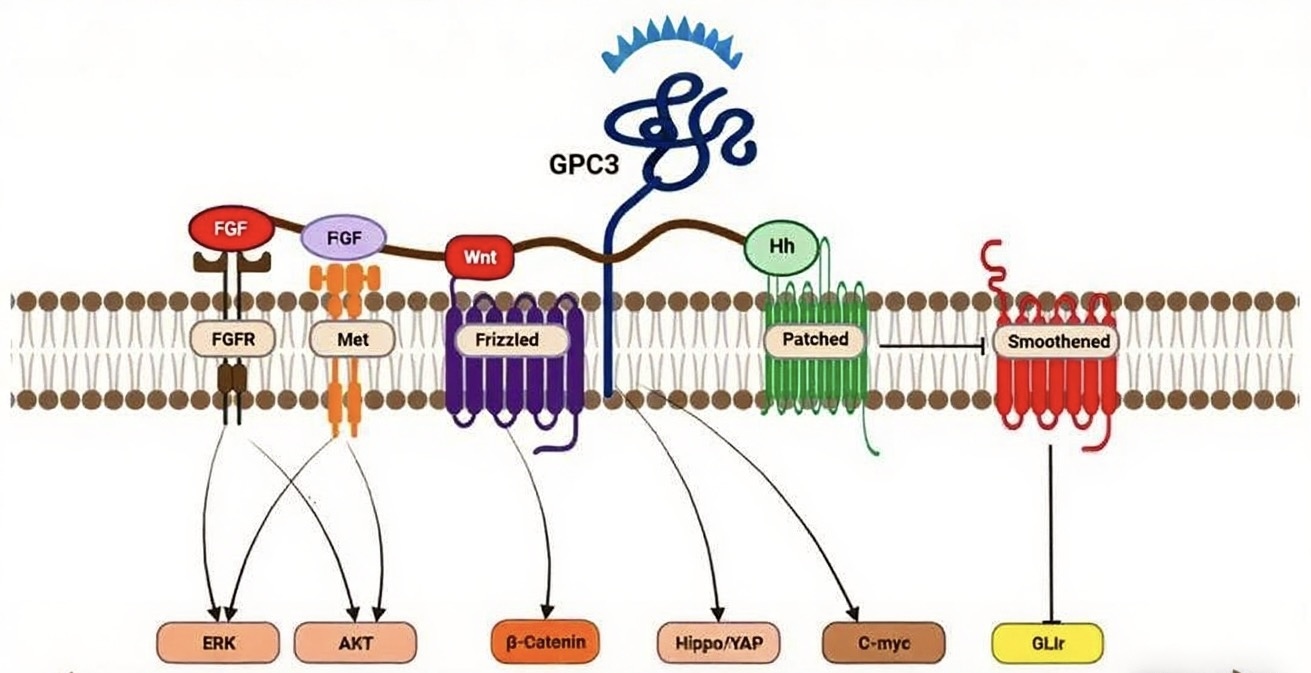
3. 为什么GPC3被视为肝癌靶向治疗的理想靶点?
GPC3在正常成人组织中几乎不表达,而在肝细胞癌中显著高表达,约70%–80%的HCC病例呈现GPC阳性。这种高度选择性的表达模式使其成为肝癌精准治疗的理想靶点,可大幅降低对正常组织的脱靶毒性。此外,GPC3通过多种机制促进肝癌进展,包括增强细胞增殖、抑制凋亡、诱导血管生成等,针对该靶点的干预有望从多维度抑制肿瘤发展。
4. 目前哪些GPC3靶向疗法处于研究和临床阶段?
目前以GPC3为靶点的治疗方法呈多元化发展,主要包括以下几类:
免疫毒素:将GPC3抗体与毒素分子偶联,精准递送细胞毒药物;
CAR-T细胞疗法:通过基因工程改造T细胞,使其表达靶向GPC3的嵌合抗原受体;
TCR-T疗法:优化T细胞受体以识别GPC3抗原肽-MHC复合物;
单克隆抗体及双特异性抗体:如Erlotinib衍生物及GPC3xCD3双抗;
肿瘤疫苗:基于GPC3抗原表位的预防性与治疗性疫苗。
多项Ⅰ/Ⅱ期临床试验已展开,尤其在CAR-T领域,中国和研究团队已报道了令人鼓舞的早期临床结果。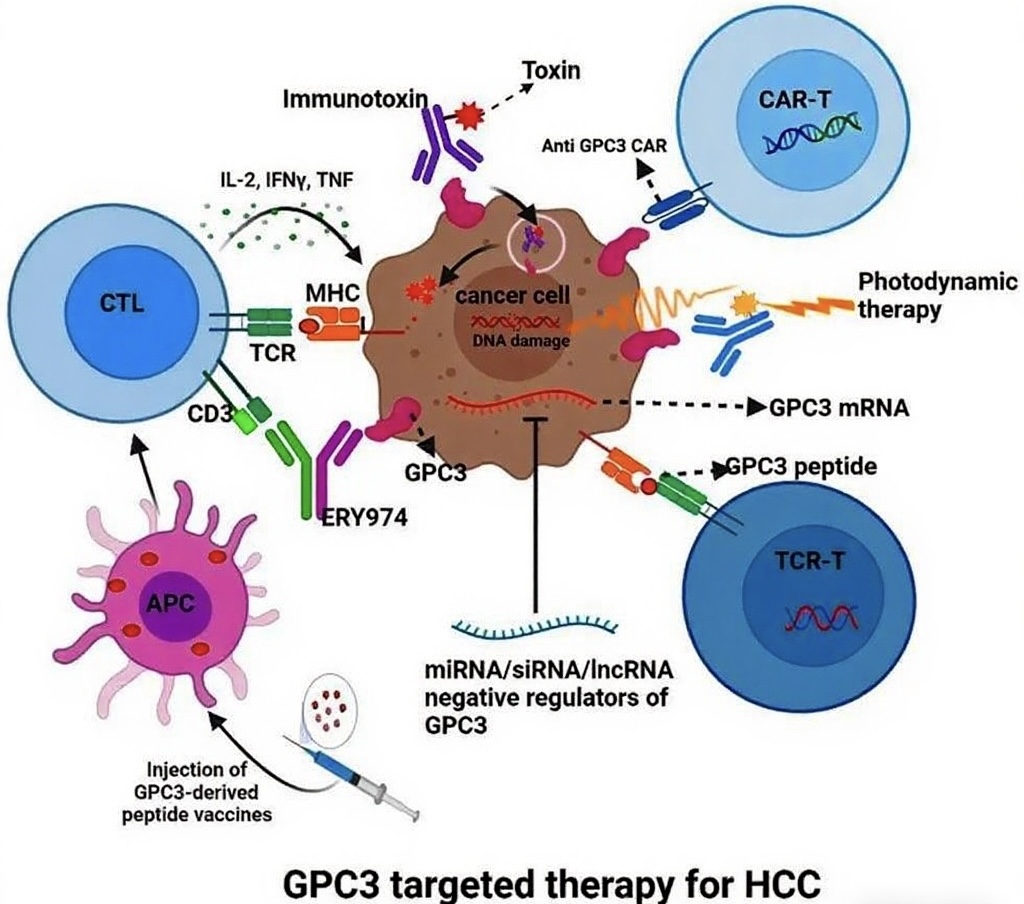
5. GPC3-CAR-T治疗肝癌的临床进展如何?
GPC3-CAR-T疗法是目前HCC免疫治疗的热点。已有临床试验显示,靶向GPC3的CAR-T细胞在晚期肝癌患者中表现出可接受的安全性及初步疗效。例如,在某些研究中,患者经历肿瘤缩小或疾病稳定,且细胞输注后细胞因子释放综合征(CRS)可控。优化策略也在不断推进,包括引入安全开关、联合免疫调节药物、开发第四代CAR-T等,旨在提高其持久性和抗肿瘤效果。
6. GPC3在肝癌以外的肿瘤或疾病中是否有表达?
尽管GPC3在绝大多数正常组织中沉默,但在某些胚胎组织(如胎盘、胚胎肝)及少数肿瘤类型(如黑色素瘤、卵黄囊瘤、部分肺鳞癌)中也检测到其表达。此外,GPC3基因突变与Simpson-Golabi-Behmel综合征(一种罕见的X连锁遗传病)相关,表现为组织过度生长和多器官异常。这些发现提示GPC3在发育及疾病中具有多重生物学功能。
7. 未来GPC3靶向治疗面临哪些挑战与方向?
尽管前景广阔,GPC3靶向治疗仍面临诸多挑战:
肿瘤异质性导致靶点表达不均;
免疫细胞肿瘤浸润能力不足;
肿瘤微环境抑制免疫应答;
治疗耐药机制的出现。
未来研究将致力于开发更高效的递送系统、联合疗法(如与免疫检查点抑制剂联用)、以及基于生物标志物的患者分层策略,以提升治疗响应率与生存获益。












